Universidad UNAD
La Universidad Nacional Abierta y a Distancia, (UNAD) es un ente universitario autónomo del orden nacional con régimen especial
Está vinculado al Ministerio de Educación Nacional en lo que a políticas y planeación del sector educativo se refiere, cuyo objetivo principal es la educación abierta y a distancia y anualmente ingresan alrededor de 7000 u 8000 estudiantes a esta institución.
Está universidad se creó con el objetivo de implementar programas académicos ,que fuesen adecuados a las necesidades locales, regionales, nacionales e internacionales. Tiene una dinámica con fines científicos, sociales y culturales.
 En abril de 1982 la Universidad empezó a funcionar y su mayor característica es tener compromiso y disciplina esto ha llevado a que la universidad tenga una alta calidad. Ella da muchas oportunidades a las poblaciones con capacitaciones técnicas, comunitarias y socio-humanísticas, esta genera espacios laborales donde ayuda a que haya participación ciudadana y estas personas se beneficien con los sueldos de estas.
En abril de 1982 la Universidad empezó a funcionar y su mayor característica es tener compromiso y disciplina esto ha llevado a que la universidad tenga una alta calidad. Ella da muchas oportunidades a las poblaciones con capacitaciones técnicas, comunitarias y socio-humanísticas, esta genera espacios laborales donde ayuda a que haya participación ciudadana y estas personas se beneficien con los sueldos de estas.
La universidad UNAD cuenta con programas académicos de pregrado y posgrado, estas se clasifican así:
- Administrativas, Contables, Económicas y de Negocios: Estas cuentan con Maestrías, Especializaciones, Profesionales y Tecnologías.
- Agrícolas, pecuarias y del Medio Ambiente: Estas cuentan con Especializaciones, Profesionales y Tecnologías.
- Ciencias básicas, Tecnologías e Ingeniería: Maestrías, Especializaciones, Profesionales y Tecnologías.
- Educación: Profesionales y Tecnologías.
- Sociales, Artes y Humanidades: Maestrías y Profesionales.
- Salud: Profesionales y Tecnologías
- Ciencias Politicas y juridicas: Especializaciones.
Problemática Ambiental, Mundial.
- Calentamiento global.
El calentamiento global es el aumento de la temperatura del proceso de la media de los océanos y la atmósfera de la Tierra causada por las emisiones que realzan el efecto invernadero, se originó a partir de una serie de actividades humanas, especialmente la quema de combustibles fósiles y los cambios en el uso del suelo, tales como la de-forestación.
Específicamente es un aumento de la temperatura media de la superficie terrestre, considerado como un síntoma y una consecuencia del cambio climático.
 |
Estos son los elementos necesarios para subsistir.
|
- Causas del calentamiento global.
En el caso de las causas naturales, han estado contribuyendo al calentamiento global del planeta desde hace miles y miles de años. Sin embargo, este tipo de causas no son los suficientemente importantes para dar lugar a los cambios climáticos que está sufriendo todo el planeta a día de hoy y que están provocando una seria amenaza para el mundo entero y estas son:
Emisión de gases de efecto invernadero: La absorción de energía por un determinado gas tiene lugar cuando la frecuencia de la radiación electromagnética es similar a la frecuencia vibracional molecular del gas. Cuando un gas absorbe energía, esta se transforma en movimiento molecular interno que produce un aumento de temperatura.
Vapor de agua en la atmósfera: Lo que provoca que la temperatura media vaya en aumento cada cierto tiempo y contribuyendo al propio calentamiento. Por su abundancia es el gas de efecto invernadero de mayor importancia, jugando un rol de vital importancia en el balance energético global de la atmósfera. La extensión real de su efecto se ha debatido bastante
El gran problema de los terremotos es que se pueden prever pero con un rango de tiempo muy amplio y, cuando ocurren en zonas muy pobladas, el impacto es enorme.
En el caso de las causas artificiales el hombre ha ayudado a que el medio ambiente sea destruido poco a poco y ha no tomar conciencia sobre esta problemática tan grave que estamos viviendo. Entre estas están:
-
La deforestación: El hombre con la deforestación, la explotación de los suelos y la quema de combustibles fósiles libera grandes cantidades de dióxido de carbono, lo que aumenta considerablemente su concentración en la atmósfera.
Quema de combustibles fósiles (hidrocarburos): Investigadores del Laboratorio Nacional Lawrence-Livermore realizaron un simulador del clima y del ciclo del carbono. Este modelo científico estimó que habrá un aumento gradual de 8°C en la temperatura del planeta hasta el año 2300 si se continuan utilizando combustibles fósiles.
- Consecuencias del calentamiento global.
Temperaturas más cálidas: La acumulación de gases contaminantes hace que las temperaturas aumenten cada vez más y que los climas cambien: esto provoca sequías y, además, aumenta el riesgo de incendios que conlleva la deforestación y la desertización del planeta.
 En 2012, los países del Sahel, en el norte de África, sufrieron una crisis alimentaria que afectó a unos 18 millones de personas debido a la escasez de lluvias. Los efectos de la sequía no son nuevos en esta zona, que viene sufriendo sequías recurrentes de forma periódica pero sí lo son la intensidad y la frecuencia de las mismas, que se han incrementado durante la última década como consecuencia del aumento de las temperaturas en el planeta.
En 2012, los países del Sahel, en el norte de África, sufrieron una crisis alimentaria que afectó a unos 18 millones de personas debido a la escasez de lluvias. Los efectos de la sequía no son nuevos en esta zona, que viene sufriendo sequías recurrentes de forma periódica pero sí lo son la intensidad y la frecuencia de las mismas, que se han incrementado durante la última década como consecuencia del aumento de las temperaturas en el planeta.
Tormentas más intensas: El hecho de que las temperaturas sean más altas hace que las lluvias sean menos frecuentes, pero que sean más intensas; por tanto, el nivel de inundaciones y su gravedad también irán en aumento.
Propagación de enfermedades: Un cambio de temperatura de varios grados puede hacer que la zona templada se haga más acogedora a la propagación de determinadas enfermedades. De esta manera, pueden empezar a darse casos de mal de Chagas, el dengue u otras enfermedades que están olvidadas en los países desarrollados y en zonas que tradicionalmente han sido más frías.
Este hecho afecta también a los países en desarrollo. Un estudio de casos en Etiopía realizado por científicos de las universidades de Denver (UD) y Michigan (UM), concluyó que el aumento de un solo grado en la temperatura del ambiente tiene como consecuencia el desarrollo de 3 millones de casos de malaria más en Etiopía en pacientes de menos de 15 años.
Olas de calor más fuertes:El calentamiento global del planeta producido por la quema acelerada de combustibles fósiles agotables ha sido muy intenso en el Polo Norte. Esto hace que el Polo Norte este hoy mucho más caliente que hace cincuenta años. La salud e incluso la vida de miles de personas pueden verse en riesgo debido al aumento de las olas de calor, tanto en lo que se refiere a frecuencia como a intensidad.
Derretimiento de los glaciares: Océanos con temperaturas más altas son océanos que derriten el hielo de los casquetes polares: esto significa que aumenta el nivel del mar.
Huracanes más peligrosos: El aumento de temperatura del mar hace que los huracanes se vuelvan más violentos.¿Por qué? Pues porque un huracán es el medio que tiene el planeta para repartir el exceso de calor de las zonas cálidas a las más frías. Y a más temperatura, más huracanes, con todos los problemas que conllevan: destrucción de ciudades, de cultivos, desmantelamiento de todos los sistemas, enfermedades…
Cambio de los ecosistemas: El calentamiento global del planeta producido por la quema acelerada de combustibles fósiles agotables ha sido muy intenso en el Polo Norte. Esto hace que el Polo Norte está hoy mucho más caliente que hace cincuenta años. La salud e incluso la vida de miles de personas pueden verse en riesgo debido al aumento de las olas de calor, tanto en lo que se refiere a frecuencia como a intensidad.
Desaparición de especies animales: Muchas especies de animales están viendo cómo su clima actual desaparece y no son capaces de adaptarse a cambios tan rápidamente. Así, muchos osos polares están muriendo ahogados porque no pueden alcanzar los hielos flotantes, y las aves migratorias están perdiendo la capacidad de emigrar porque no pueden seguir los flujos de temperatura a las que están habituadas.
Aumento del nivel del mar: Como los casquetes se derriten, se vierte muchísima más agua en los mares y océanos y, por tanto, aumenta el nivel del mar: esta es una de las consecuencias del cambio climático más graves, ya que significa que muchísimas islas podrían desaparecer en el futuro y que un buen número de ciudades verán cómo su distancia a la costa se reduce de forma significativa.
Alimentos más caros:El cambio climático pone en peligro la producción de alimentos tan básicos como el trigo, y esto significa que cientos de miles de personas cuya vida depende de sus cultivos están en riesgo de perderlo todo. Y no solo eso: si los cultivos escasean, los precios se disparan. Esto nos afecta a todos, pero en los países menos desarrollados, con altísimos índices de pobreza, las consecuencias pueden ser devastadoras.
Desarrollo sostenible : El desarrollo sostenible , se basa principalmente de la generación actual y esta se considera como principal rector para el desarrollo mundial a largo plazo y tiene tres pilares los cuales son
- Desarrollo económico
- Desarrolllo social
- Protección del medio ambiente
- Cómo evitar que el calentamiento global se siga expandiendo:
1. Cambia las bombillas 2.Apaga la tele y el pc
3. Recicla 4. Maneja bicicleta
5. Menos agua caliente 6. Planta un árbol
Actividades interactivas
RECOMENDACION...
Luisa Perez
Laura vargas
11.1


























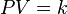
 es constante si la temperatura y la masa del gas permanecen constantes.
es constante si la temperatura y la masa del gas permanecen constantes.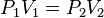




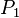 = Presión Inicial
= Presión Inicial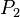 = Presión Final
= Presión Final = Volumen Inicial
= Volumen Inicial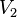 = Volumen Final
= Volumen Final












